Projektbereich E:
E1Plattform Wirkstofftestung gegen Helminthen
Simone Häberlein, Christoph Grevelding
PD Dr. Simone Häberlein
Justus-Liebig-Universität Gießen
BFS, Institut für Parasitologie
Schubertstraße 81
35392 Gießen
Tel.: +49 (0)641-99 38476
Fax: +49 (0)641-99 38469
E-Mail: Simone.Haeberlein(at)vetmed.uni-giessen(dot)de
Prof. Dr. Christoph Grevelding
BFS, Institut für Parasitologie
Justus-Liebig-Universität Gießen
Schubertstraße 81
35392 Gießen
Tel.: +49 (0)641-99 38466
Fax: +49 (0)641-99 38469
E-Mail: Christoph.Grevelding(at)vetmed.uni-giessen(dot)de
Projektbeschreibung
Targetstrukturen anti-parasitärer Substanzen sind oft konserviert, was die Möglichkeit der Therapie unterschiedlicher Parasitosen mit demselben Wirkstoff eröffnet. Im Plattformprojekt E1 fokussieren wir uns auf verschiedene parasitäre Würmer (Helminthen), für die eine Entwicklung neuer Wirkstoffe aufgrund von Resistenzen bzw. suboptimaler Therapieerfolge hohe Dringlichkeit hat. Dazu führen wir in vitro-Screenings von Substanzen aus DRUID-Projekten u.a. gegen den Bilharzioseerreger Schistosoma mansoni und den Leberegel Fasciola hepatica durch. Das Plattformprojekt verfügt über zahlreiche nationale und internationale Kooperationspartner und -partnerinnen, auch in endemischen Ländern in Asien und Afrika, die uns Testmöglichkeiten gegen eine Vielzahl weiterer Helminthenspezies ermöglichen.
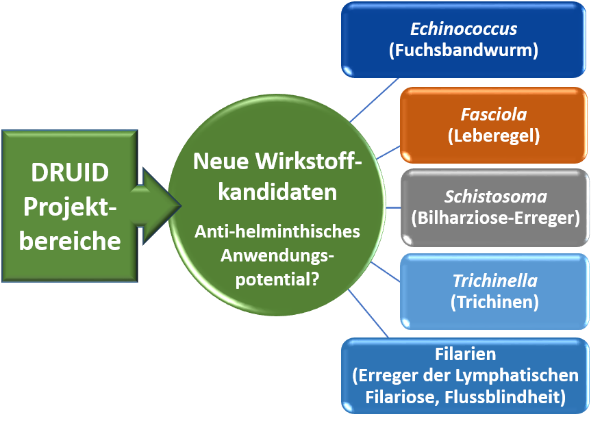
Strategie zur Identifizierung von Substanzen mit breitem Wirkspektrum gegenüber weltweit wichtige Helminthen-arten. ©Simone Häberlein
Für ausgewählte Substanzen werden zudem Wirkmechanismus-Analysen durchgeführt, wobei verschiedene in-vitro-Kultur-basierte und bildgebende Methoden zum Einsatz kommen.
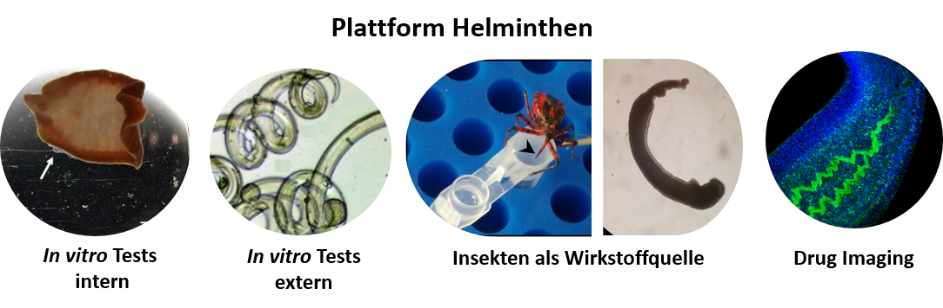
Testmöglichkeiten des Helminthen-Plattformprojekts für Wirkstoffkandidaten. ©Simone Häberlein, Miray Tonk-Rügen
Wissenschaftliches Ziel:
Ziel des Projekts ist die Identifizierung von Substanzen mit breitem anti-parasitären Wirkspektrum sowie die Aufklärung konservierter Wirkmechanismen.
DRUID-Kooperationspartner:
A2 Grünweller lab, A6 Douglas lab, A7 Przyborski lab, B4 Schlitzer lab, B5 Grevelding lab, B7 Falcone lab, E4 Spengler lab
Literatur E1: 1. Peter-Ventura et al. (2019) ChemMedChem 14(21):1856-1862. 2. Houhou et al. (2019) Sci Rep 9:15867. 3. Li et al. (2019) Parasitol Res 118(3):881-890. 4. Morawietz et al. (2020) Front Vet Sci 7:611270. 5. Kellershohn et al. (2019) PLOS Negl Trop Dis 13:e0007240. 6. Tonk et al. (2020) Antibiotics 9:664. 7. Mokosch et al. Anal Bioanal Chem 413(10): 2755-2766. 8. Mughal et al. (2021a) Int J Parasitol 51(7):571-585. 9. Mughal et al. (2021b) Int J Parasitol S0020-7519(21)00312-X. 10. Gallinger et al. (2022) Pharmaceuticals 15(2): 119. 11. Morawietz et al. (2022) Parasitol Res (online ahead of print) doi: 10.1007/s00436-021-07388-1
E3Proteinproduktion, HTS-Assays, Kristallisation, Interaktionsanalysen
Jude Przyborski, Stefan Rahlfs
Prof. Dr. Jude Przyborski
Interdisziplinäres Forschungszentrum (iFZ)
Justus-Liebig-Universität Gießen
Heinrich-Buff-Ring 26-32
35392 Gießen
Tel.: +49 (0)641-99 39114
E-Mail: jude.przyborski(at)ernaehrung.uni-giessen(dot)de
Dr. Stefan Rahlfs
Biochemie und Molekularbiologie
Justus-Liebig-Universität Gießen
Heinrich-Buff-Ring 26-32
35390 Gießen
Tel.: +49 (0)641-99 39117
E-Mail: stefan.rahlfs(at)ernaehrung.uni-giessen(dot)de
Projektbeschreibung
Rahmen der Plattform [E3] sollen Methoden zur Proteinproduktion, zur Entwicklung von high-throughput Assays, zur Kristallisation und Strukturanalyse sowie zu Interaktionsanalysen für das DRUID-Konsortium bereitgestellt werden. Dabei kann eine Vielzahl an Optimierungsmöglichkeiten bei der Klonierung/Expression sowie bei der Reinigung nativer Proteine (Affinitäts-chromatographie, Gelfiltration, Ionenaustauscher) angeboten werden. Für erfolgreich rekombinant produzierte Proteine kann über die Plattform [E3] Unterstützung bei der Entwicklung von Assaysystemen bis hin zu high throughput-fähigen Formaten gegeben werden. Des Weiteren soll über das Projekt [E3] Zugang zu der Kristallisationsplattform am iFZ ermöglicht werden. Für Kristallisationscreens im nl-Massstab stehen ein Pipettier- sowie ein Kristallisationsroboter sowie Starterkits und diverse Additivscreens zur Optimierung zur Verfügung, z. Z. wird das System durch Finanzierung von DRUID erneuert. Frau Dr. Fritz-Wolf wird als Kristallografin und Ansprechpartnerin fungieren und kann die ersten Testungen der Kristalle vornehmen. Hierzu stehen die Röntgenquellen des Max-Planck-Instituts für Med. Forschung (Heidelberg) bzw. der AG Klebe/Heine [A5] (Marburg) zur Verfügung.
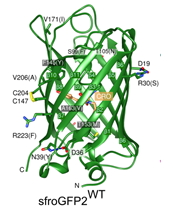
Struktur von sfroGFP (Heimsch et al. 2022)
DRUID-Kooperationspartner:
Im Bereich Protein-Expression: A1, A3, A6NWG, A7, B2, B3, B4, C3
Im Bereich Kristallisation: B2, B3, C3
Im Bereich Assay-Entwicklung: A7, B3
Literatur E3: 1. Heimsch et al. (2022) Antioxid & Redox Signal doi: 10.1089/ars.2021.0234 2. Harnischfeger et al. (2020) Electronic Journal of Biotechnology 3. Fritz-Wolf et al. (2011) Nat Commun 2:383 4. Koncarevic et al. (2009) Proc Natl Acad Sci USA 106:13323-8
E4Hochauflösende, bildgebende Massenspektrometrie
Bernhard Spengler
Prof. Dr. Bernhard Spengler
Institut für Anorganische und Analytische Chemie
Justus-Liebig-Universität Gießen
Heinrich-Buff-Ring 17
35392 Gießen
Tel.: +49 (0)641-99 34801
E-Mail: bernhard.spengler(at)ac.jlug(dot)de
Projektbeschreibung
Die hochauflösende, bildgebende Massenspektrometrie bietet vielfältige Einsatz–möglichkeiten, bei der Untersuchung von Pathogenen, der Pathogen-Wirts-Wechselwirkung sowie der Charakterisierung von Wirkstoffen. Die zu untersuchende Probe wird mithilfe eines Lasers abgerastert, die Schrittweite beträgt wenige Mikrometer. Hierbei wird Probenmaterial abgetragen und ionisiert, dies erlaubt die parallele Detektion hunderter chemischer Verbindungen sowie die bildliche Darstellung der Verteilung dieser Verbindungen in der Probe. Die Identifizierung der Moleküle erfolgt durch hochpräzise Messung der Ionenmasse in Verbindung mit Fragmentierungsexperimenten. Durch kontinuierliche Verbesserung der Ionisierungsmethode können immer kleinere Strukturen dargestellt und niedrig konzentrierte Analyten durch beispielweise in-situ Derivatisierung detektiert werden.
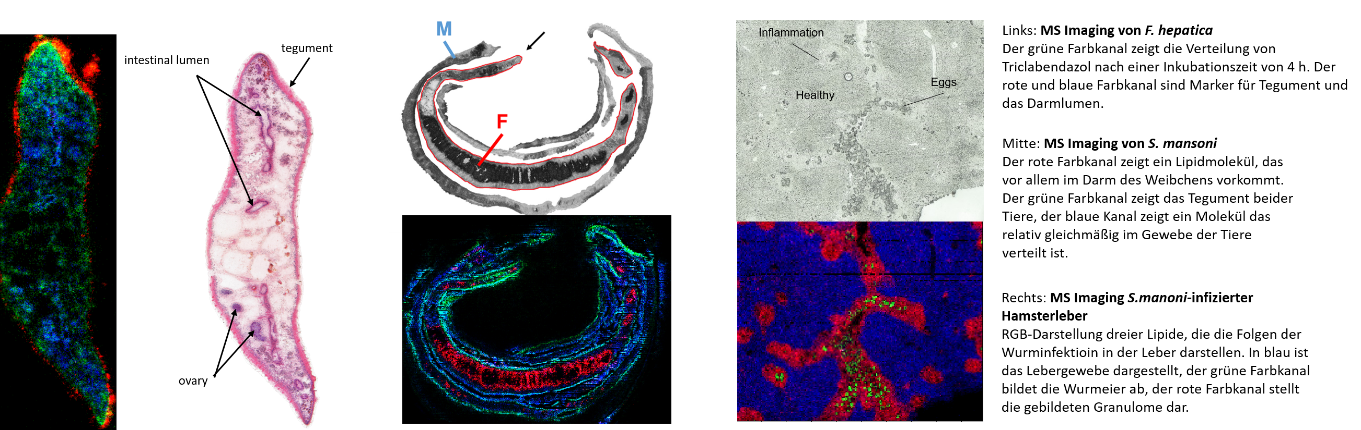
Wissenschaftliches Ziel:
Das Ziel des Projekts ist die Verbesserung und Anwendung der vorhandenen Methoden auf Fragestellungen innerhalb des DRUID Zentrums. Wichtige Forschungsfelder sind insbesondere die Verteilung von Wirkstoffen, lipidomische und metabolomische Charaktierisierung von Pathogenen und die Pathogen-Wirts-Interaktion.
DRUID-Kooperationspartner:
A2 Grünweller lab, B4 Grevelding lab, B5 Schlitzer lab, D4 Taubert lab, E1 Häberlein lab, W3 Herker lab
Literatur E4: [1] Kadesch et al. (2020) PLoS Negl. Trop. Dis. 14(5): e0008145; [2] Morawietz et al. (2020), Front. Vet. Sci. 7, 611270; [3] Mokosch et al. (2021) Anal Bioanal Chem 413, 2755–2766; [4] Müller et al. (2021) J. Am. Soc. Mass Spectrom.,3,32(2),465-472; [5] Spengler et al. (2015) Anal Chem 87 (1) 64-82.
E5Prozessentwicklung/-kontrolle (PAT, cGMP), Plattformen für die Produktion von Proteinen und Virusähnlichen Partikeln
Peter Czermak, Denise Salzig
Prof. Dr. Ing. Peter Czermak
Institut für Bioprozesstechnik
Technische Hochschule Mittelhessen
Wiesenstraße 14
35390 Gießen
Tel.: +49 (0)641-309 2551
E-Mail: peter.czermak(at)lse.thm(dot)de
Prof. Dr. Ing. Denise Salzig
Institut für Bioverfahrenstechnik
und Pharmazeutische Technologie
Technische Hochschule Mittelhessen
Gutfleischstr. 3-5
Tel.: +49 (0)641-309 2630
Fax: +49 (0)641-309 2553
E-Mail: denise.salzig(at)lse.thm(dot)de
Projektbeschreibung
Um Forschungsergebnisse aus dem DRUID Konsortium in die Klinik oder die Industrie zu translatieren, sind robuste Produktionsprozesse, die mehr als eine bloße Maßstabsvergrößerung darstellen, unabdingbar. Dabei müssen diese Prozesse den Richtlinien der guten Herstellungspraxis (cGMP) und der Prozessanalytischen Technologie (PAT) folgen. Folgende Arbeiten sind geplant: i) Prozessintensivierung und Ausbau der BEVS-Produktionsplattform sowie Umsetzung einer kontinuierlichen Prozessführung, ii) Einbindung von online PAT-Technologie, z.B. Impedanzspektroskopie zur automatischen Bestimmung des optimalen Erntezeitpunkts und der automatisierten Ernte, iii) Expression (BEVS) und Aufreinigung von S. mansoni-Kinasen sowie Untersuchung der Kinasen und putativer Inhibitoren, und iv) Untersuchung neuartiger Transfektionsreagenzien für die transiente Proteinproduktion im Bioreaktormaßstab.
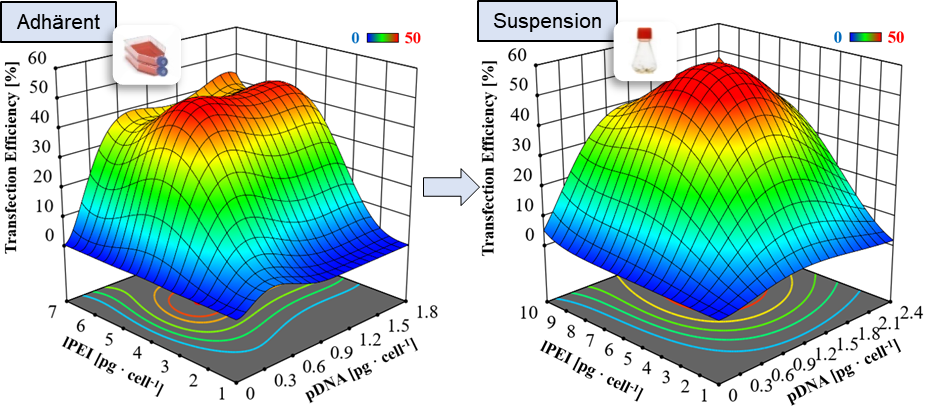
Optimierung des transienten Transfektionsprozesses mittels statistischer Versuchsplanung. ©IBPT
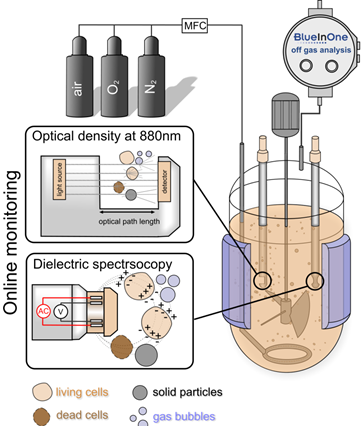
Produktionskonzept mit integrierter PAT-Technologie. ©IBPT
Wissenschaftliches Ziel:
Die Arbeiten zur Produktionsprozessentwicklung und Prozessanalytik werden weiter an die Fragestellungen des Zentrums angepasst, erweitert, und dem gesamten Konsortium zur Nutzung angeboten. Insbesondere ist geplant, die aufgebaute BEVS (Baculovirus-Expression-System)-Plattform weiter zu intensivieren und zu automatisieren. Darüber hinaus wird auch die zweite Produktionsplattform – die transiente Produktion mit HEK-293T-Zellen – weiterentwickelt.
DRUID-Kooperationspartner:
B4 AG Schlitzer, B5 AG Grevelding, B7 P AG Falcone, C6 NWG Häberlein, E1 Plattform Grevelding/Häberlein
Literatur E5: Biotechnol, DOI: 10.1016/j.ejbt.2021.08.002, 3. Lothert et al. (2020) Methods Mol Biol 2183:217-248, 4. Dekevic et al. (2022) J Biotechn 346 23-34, 5. Schwarz et al. (2021) Elec J Biotechnol, DOI: 10.1016/j.ejbt.2022.01.003; 6. Barekzai et al. (2020) New Adv Ferm Processes, DOI: 10.5772/intechopen.90029, 7. Eckhardt et al. (2021) Sep Sci Technol, 57 (6) 886-897
E6Pharmazeutische Entwicklung, Translationale Medizin, drug repurposing
Susanne Schiffmann
Dr. Susanne Schiffmann
Fraunhofer Institut für Translationale Medizin und Pharmakologie ITMP
Theodor-Stern-Kai 7
60596 Frankfurt am Main
Tel.: +49 (0)69-8700 25060
E-Mail: susanne.schiffmann(at)itmp.fraunhofer(dot)de
Projektbeschreibung
Die SARS-CoV2-Pandemie verdeutlicht, dass die Entwicklung von Arzneimitteln, die Infektionen therapieren können, dringend notwendig ist. Um neue Behandlungsoptionen zu identifizieren, werden vielversprechende Substanzen aus anderen Arbeitsgruppen präklinisch charakterisiert. Dies umfasst die Erstellung eines Sicherheitsprofils sowie die Bioverfügbarkeitstestung der Wirkstoffkandidaten. Da eine unterstützende Therapie mit immunmodulierenden Arzneimitteln einen bewährten Therapieansatz darstellt, wird eine Interaktion der Wirkstoffkandidaten mit dem Immunsystem geprüft.
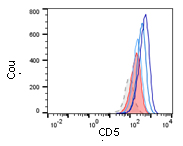
Veränderung der Oberflächenmarker-expression auf behandelten M2-Makrophagen ©Marina Henke
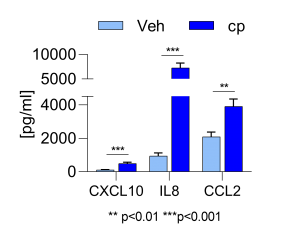
Veränderung der Zytokinfreisetzung in behandelten M2-Makrophagen ©Leonard Blum
Wissenschaftliches Ziel:
Im Rahmen des Projektes soll für small molecules/Peptide, die potenziell eine antivirale, antiparasitäre oder antibakterielle Wirkung haben, ein Sicherheits- und/oder immunmodulatorisches Profil erstellt werden. Des Weiteren werden in diesem Projekt humane Zielproteine (z. B. TMPRSS2) untersucht, die neue Targets zur Bekämpfung von Pathogenen darstellen.
DRUID-Kooperationspartner:
A1 Becker lab, A2 Grünweller lab, A3 Weber lab, B1 Diederich/Kolb lab, B3 Rahlfs/Kolb/van Zandbergen, B5 Schlitzer lab, D1 Friebertshäuser lab
Literatur E6: 1. Blum et al. (2021) J Mol Med 99(2):261-72; 2. Blum et al. (2020) Sci Rep 10(1):7534; 3. Blum et al. (2020) J Cell Mol Med 24(12):6988-99.
E7 PVernachlässigte Infektionskrankheiten mit Schwerpunkt bildgebender Verfahren
Jacomina Krijnse Locker
Prof. Dr. Jacomina Krijnse Locker
Elektronenmikroskopie von Pathogenen
Paul-Ehrlich-Institut
Paul-Ehrlich-Straße 51-59
63225 Langen
Tel.: +49 (0)6103-77 2011
E-Mail: Jacomina.KrijnseLocker(at)pei(dot)de
Projektbeschreibung
Wir setzen bildgebende Verfahren ein, um zu verstehen wie Krankheitserreger mit der Wirtszelle interagieren und Krankheiten verursachen. Unser Fokus liegt auf der Elektronenmikroskopie (EM) und korrelativer Licht- und Elektronenmikroskopie (CLEM). Um robuste, anpassbare Protokolle zu generieren, verwenden wir das große DNA-Virus Vaccinia (VACV) als Modell. Die SARS-CoV2-Pandemie veranschaulicht, wie Viren weltweit sozioökonomische Auswirkungen mit dramatischen Folgen für die vernachlässigten Tropenkrankheiten (NTDs) haben. Es besteht die dringende Notwendigkeit, die SARS-CoV2-Pandemie einzudämmen und die Ressourcen auf NTDs zu konzentrieren. In einer Instituts-übergreifenden Kooperation haben wir gezeigt, dass das Spike- Protein (S) von SARS-CO-2, das essenziell für die Infektion ist, eine unerwartete Flexibilität aufweist. Dies könnte die Rezeptorbindung und den Zelleintritt des Virus erleichtern, was bis jetzt nicht bewiesen ist.
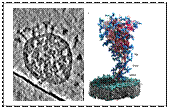
Die Kryoelektronentomographie von SARS-CoV-2 und die molekulare dynamische Simulation des Spike Proteins zeigen eine unerwartete Flexibilität des Stiels.
Nach der Knospung (Entstehung der Virushülle) an der intrazellulären Membranen verlassen Coronaviren die Zelle auf eine bisher wenig erforschte Weise. Vesikuläres Trafficking sowie eine regulierte lysosomale Exozytose werden dabei als Mechanismen diskutiert.
Wissenschaftliches Ziel:
Ziel des Projektes ist es, mit Hilfe von Antikörpern, Medikamenten und Genetik in die Flexibilität von S einzugreifen, Auswirkungen auf die Infektion zu testen und damit die Funktion zu verstehen. Die Virusfreisetzung aus infizierten Zellen soll mit einem CLEM-Ansatz untersucht werden, der Live-Cell-Imaging mit EM kombiniert. Die aus unserem VACV- und SARS CoV2-Wirtssystem gewonnene Expertise kann dann zur Beantwortung von Fragen im Kontext anderer Virus-Wirtssystemen der Teams des DRUID-Konsortiums eingesetzt werden.
DRUID-Kooperationspartner:
A3 Weber lab, B2 Ziebuhr lab, B6 P Herker lab, C1 Hildt lab, D3 van Zandbergen lab, E5 Czermak lab
Literatur E7 P: Turoňová, B., et al. (2020). Science (80-. ). 370, 203–208. Blanco-Rodriguez, G., et al.(2020). J. Virol. 94 e00135-20. Quemin, E.R., et al. (2018). J. Mol. Biol.430, 1714-1724. Chlanda, P., and Krijnse Locker, J. (2017). Biochem. J. 474, 1041–1053. Sartori-Rupp, A., et al. (2019). Nat. Commun. 10, 342.









