Projektübersicht
Prof. Dr. Stephan Becker
Institut für Virologie
Philipps-Universität Marburg
Hans-Meerwein-Str. 2
35043 Marburg
Phone: +49 (0)6421-28 66253
E-Mail: becker(at)staff.uni-marburg(dot)de

Interaktionen von Ebola-Virus-Proteinen als Ziele antiviraler Strategien
Projektbeschreibung
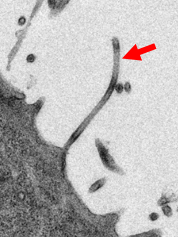
Elektronenmikroskopische Aufnahme von Ebolavirus infizierten Zellen. Die langgestreckten Viruspartikel werden von der Oberfläche der Zelle freigesetzt (roter Pfeil). ©Schauflinger
Das Ebolavirus (EBOV) verursacht schweres Fieber mit einer außerordentlich hohen Sterblichkeit. Das Matrixprotein VP40 von EBOV spielt eine Schlüsselrolle im viralen Replikationszyklus, der durch Homooligomerisierung des Proteins gesteuert wird. Die Dimerisierung von VP40 ist entscheidend für den Transport des Proteins zur Plasmamembran, wo die Dimere polymerisieren und zur Bildung von Filamenten führen, die die Knospung des Virus ermöglichen. Die VP40-Oktamerisierung führt zu einer Herunterregulierung der viralen RNA-Synthese. Aufgrund ihrer zentralen Rolle als Bausteine von Oligomeren höherer Ordnung stellen Dimere ein vielversprechendes Ziel für antivirale Medikamente dar. Mit Hilfe eines fragmentbasierten Ansatzes wurden kleine Moleküle identifiziert, die an VP40-Kristalle binden und zu Leitverbindungen weiterentwickelt werden sollen, um die VP40-Oligomerisierung und damit die Virusreplikation zu hemmen.
Hochauflösende Kristallstruktur des dimerischen Matrixproteins VP40 des Ebolavirus. ©Anke Werner
Wissenschaftliches Ziel:
Das Projekt zielt darauf ab, identifizierte Leitmoleküle zu antiviralen Medikamenten zu entwickeln, wobei strukturbasiertes Wirkstoffdesign – eine Kombination aus Proteinkristallographie und in silico-Methoden – sowie Zellkulturexperimente unter BSL4-Bedingungen zur Validierung eingesetzt werden.
DRUID-Kooperationspartner:
B1 Diederich/Kolb lab, A4 Heine/Reuter lab, D1 Steinmetzer lab, E3 Rahlfs/Przyborski lab
Literatur A1: 1. *Hartlieb et al. (2007) PNAS 104: 624-9 2. *Hartlieb et al., (2003) J. Biol. Chem. 278: 41830-6 3. *Hoenen et al. (2005) J Virol. 79: 1898-905 4. *Möller et al. 79, 14876-86 (2005) J Virol. 5. Hoenen et al. (2010) J Virol 84: 7053-63. 6. *Gomis-Ruth et al. (2003) Structure 11: 423-33.
