Projektübersicht
PD Dr. Simone Häberlein
Justus-Liebig-Universität Gießen
BFS, Institut für Parasitologie
Schubertstraße 81
35392 Gießen
Tel.: +49 (0)641-99 38476
Fax: +49 (0)641-99 38469
E-Mail: Simone.Haeberlein(at)vetmed.uni-giessen(dot)de

Plattform Wirkstofftestung gegen Helminthen
Projektbeschreibung
Targetstrukturen anti-parasitärer Substanzen sind oft konserviert, was die Möglichkeit der Therapie unterschiedlicher Parasitosen mit demselben Wirkstoff eröffnet. Im Plattformprojekt E1 fokussieren wir uns auf verschiedene parasitäre Würmer (Helminthen), für die eine Entwicklung neuer Wirkstoffe aufgrund von Resistenzen bzw. suboptimaler Therapieerfolge hohe Dringlichkeit hat. Dazu führen wir in vitro-Screenings von Substanzen aus DRUID-Projekten u.a. gegen den Bilharzioseerreger Schistosoma mansoni und den Leberegel Fasciola hepatica durch. Das Plattformprojekt verfügt über zahlreiche nationale und internationale Kooperationspartner und -partnerinnen, auch in endemischen Ländern in Asien und Afrika, die uns Testmöglichkeiten gegen eine Vielzahl weiterer Helminthenspezies ermöglichen.
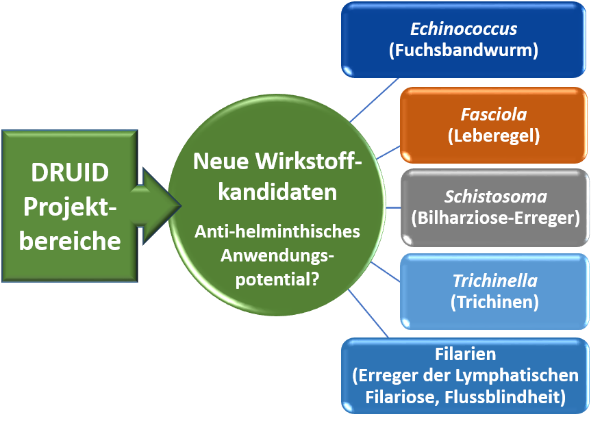
Strategie zur Identifizierung von Substanzen mit breitem Wirkspektrum gegenüber weltweit wichtige Helminthen-arten. ©Simone Häberlein
Für ausgewählte Substanzen werden zudem Wirkmechanismus-Analysen durchgeführt, wobei verschiedene in-vitro-Kultur-basierte und bildgebende Methoden zum Einsatz kommen.
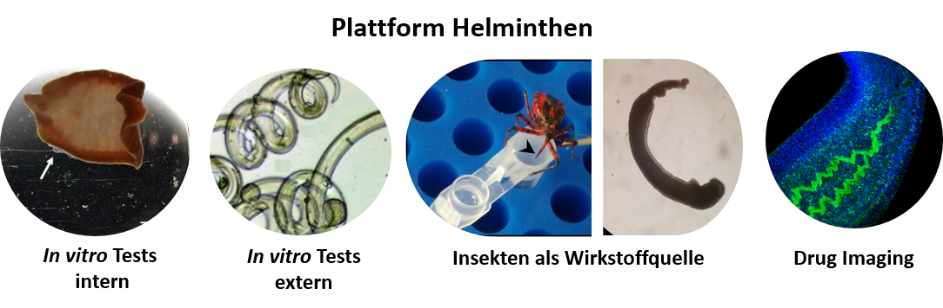
Testmöglichkeiten des Helminthen-Plattformprojekts für Wirkstoffkandidaten. ©Simone Häberlein, Miray Tonk-Rügen
Wissenschaftliches Ziel:
Ziel des Projekts ist die Identifizierung von Substanzen mit breitem anti-parasitären Wirkspektrum sowie die Aufklärung konservierter Wirkmechanismen.
DRUID-Kooperationspartner:
A2 Grünweller lab, A6 Douglas lab, A7 Przyborski lab, B4 Schlitzer lab, B5 Grevelding lab, B7 Falcone lab, E4 Spengler lab
Literatur E1: 1. Peter-Ventura et al. (2019) ChemMedChem 14(21):1856-1862. 2. Houhou et al. (2019) Sci Rep 9:15867. 3. Li et al. (2019) Parasitol Res 118(3):881-890. 4. Morawietz et al. (2020) Front Vet Sci 7:611270. 5. Kellershohn et al. (2019) PLOS Negl Trop Dis 13:e0007240. 6. Tonk et al. (2020) Antibiotics 9:664. 7. Mokosch et al. Anal Bioanal Chem 413(10): 2755-2766. 8. Mughal et al. (2021a) Int J Parasitol 51(7):571-585. 9. Mughal et al. (2021b) Int J Parasitol S0020-7519(21)00312-X. 10. Gallinger et al. (2022) Pharmaceuticals 15(2): 119. 11. Morawietz et al. (2022) Parasitol Res (online ahead of print) doi: 10.1007/s00436-021-07388-1
Das Fasciola-Kinom als Quelle für neue Wirkstofftargets
Projektbeschreibung
Proteinkinasen regulieren eine Vielzahl zellulärer Prozesse und stellen vielversprechende Ziele für Medikamente dar, nicht nur in der Krebstherapie sondern auch gegen parasitäre Infektionserreger. Beide Erkrankungen haben u.a. gemein, dass Stammzellen eine besondere Rolle beim Wachstum spielen. Unsere Hypothese ist, dass die Inhibierung ausgewählter Proteinkinasen als Therapieansatz gegen den Leberegel Fasciola hepatica genutzt werden kann, einem weltweit vorkommenden Zoonose- und NTD-Erreger. Im Rahmen des Projektes werden (1) potentielle Wirkstoffziele im Fasciola-Kinom bioinformatisch identifiziert und genetisch validiert, (2) gegen den Leberegel aktive Kinase-Inhibitoren identifiziert, sowie (3) die Wirkungsweise von Kinase-Inhibitoren mit biochemischen und bildgebenden Methoden charakterisiert.
U.a. haben wir in Kooperation mit der AG Spengler (Projekt E4) den Einsatz der bildgebenden AP-MALDI-Massenspektrometrie für “Drug Imaging” in Parasiten-gewebe etabliert und können so Aufnahmeroute, -kinetik und Wirkstofftropismus von Kinase-inhibitoren in Leberegeln unter-suchen.
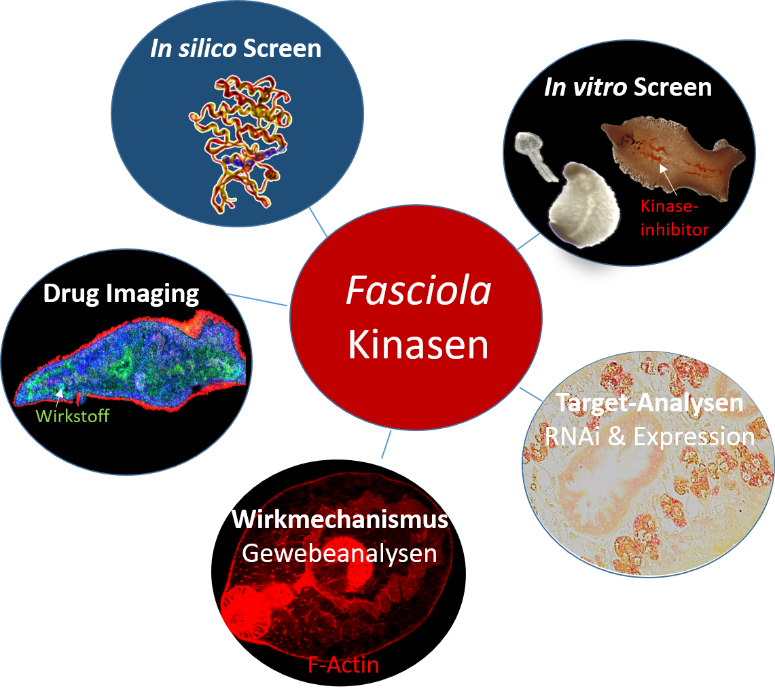
Strategie zur Identifizierung von Proteinkinase-Inhibitoren als Wirkstoffkandidat gegen den Leberegel Fasciola hepatica. ©Simone Häberlein
Wissenschaftliches Ziel:
Ziel des Projekts ist es, Proteinkinase-Inhibitoren als neue Wirkstoff-kandidaten gegen Fasciolose zu finden.
DRUID-Kooperationspartner:
A2 Grünweller lab, B4 Schlitzer lab, B5 Grevelding lab, B7 Falcone lab, E4 Spengler lab
Literatur C6: 1. Houhou et al. (2019) Sci Rep 9:15867. 2. Li et al. (2019) Parasitol Res 118(3):881-890. 3. Morawietz et al. (2020) Front Vet Sci 7:611270. 4. Mokosch et al. Anal Bioanal Chem 413(10): 2755-2766. 5. Morawietz et al. (2022) Parasitol Res (online ahead of print) doi: 10.1007/s00436-021-07388-1
