A6: Die hoch divergente Aktin-Superfamilie als Wirkstoffziel bei der Übertragung von Malariaparasiten
Dr. Ross Douglas
Biomedical Research Center Seltersberg (BFS)
Molecular Infections Biology
Justus Liebig Universität Giessen
Schubertstrasse 81
35392 Gießen
Tel.: +49 (0)641-99 39145
Fax: +49 (0)641-99 39129
E-Mail: ross.g.douglas(at)ernaehrung.uni-giessen(dot)de
Projektbeschreibung
Malaria ist nach wie vor eine der verheerendsten Krankheiten und wird durch einzellige Parasiten namens Plasmodium verursacht. Diese Parasiten werden durch Anopheles-Moskitos von Mensch zu Mensch übertragen. Der Parasit benötigt eine Reihe verschiedener Proteine, die ihm die Übertragung auf den Moskito-Vektor ermöglichen, darunter Mitglieder des stark divergierenden Aktin-Zytoskeletts und seiner Regulatoren. Das Zytoskelett des Parasiten hat einzigartige Eigenschaften, um die Übertragung zu ermöglichen. Da es für verschiedene Prozesse des Parasiten in unterschiedlichen Stadien des Lebenszyklus unerlässlich ist, enthält es vielversprechende Ziele für neuartige Malariatherapien. Wir nutzen Ansätze zur Target-Validierung, um neue Targets zu identifizieren und zu charakterisieren, die die Übertragung blockieren und zur Kontrolle der Krankheitsausbreitung eingesetzt werden könnten.
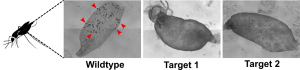
Der Ansatz der Target-Validierung hat neue Targets identifiziert, die die Übertragung blockieren.
Wissenschaftliches Ziel:
Unser Ziel ist es, die identifizierten Proteine mit in vitro und in vivo Methoden zu charakterisieren, um neue Wirkstoffe zu identifizieren, die selektiv auf diese Proteine abzielen und somit als Kandidaten für Medikamente zur Blockierung der Übertragung dienen.
DRUID-Kooperationspartner:
A7 Przyborski, B1 Diederich/Kolb, B7 P Falcone, E3 Rahlfs/Przyborski
Literatur A6: [1] Douglas et al. (2018) PLOS Bio e2005345; [2] Douglas et al. (2018) Malaria J 17:3191898-905; [3] Douglas et al. (2015) Trends Parasitol 31(8):357-362.

